瑞德西韦哪家上市公司生产?海南海药完成瑞德西韦制剂第一批生产
关于瑞德西韦哪家上市公司生产很多人还不了解,今天小编就为大家整理了相关内容,希望对各位有所帮助:
央视网消息:在昨天(25日)上午举行的国务院联防联控机制新闻发布会上,国家知识产权局副局长何志敏表示,目前,瑞德西韦在任何一个国家都还没有批准上市,现在还处于临床阶段。接下来具体说说海南海药完成瑞德西韦制剂第一批生产
被寄予厚望的瑞德西韦:博瑞医药已量产 国内掀仿制潮?
新京报讯(记者李云琦)发布成功仿制并批量生产瑞德西韦原料药的公告后,上市公司博瑞医药2月12日股价涨20%。
2月11日晚间,博瑞医药公告表示,公司近日成功仿制开发了瑞德西韦原料药合成工艺技术和制剂技术。公司已经批量生产出瑞德西韦原料药,瑞德西韦制剂批量化生产正在进行中。
此前美国媒体报道,当地确诊新型冠状病毒的患者接受一种实验药物Remdesivir(瑞德西韦)的注射后好转,瑞德西韦也因此被看做是最有可能应用于新型冠状病毒治疗的药物。
2月12日早间开盘,博瑞医药就股价大涨,*高报价52.12元/股,涨幅20.01%。
2月12日,记者联系博瑞医药了解仿制瑞德西韦相关情况,公司接线人员称,董事会秘书办公室的人不在公司,对于相关问题无法回应,“相关的情况我们公司正在准备情况说明会,对相关事宜会做进一步说明,但是现在说明会时间和形式都还没有确认,确认后会通知大家。”
博瑞医药成功仿制瑞德西韦 专利授权存重大不确定性
2月11日晚间,博瑞医药在公告中表示,公司成功开发了瑞德西韦原料药合成工艺技术和制剂技术,并已经批量生产出瑞德西韦原料药,瑞德西韦制剂批量化生产正在进行中。
瑞德西韦,一款由美国公司吉利德生产的在研药物。根据吉利德介绍,瑞德西韦证实了对非典型性肺炎(SARS)和中东呼吸综合征(MERS)的病毒病原体均有活性,瑞德西韦还被紧急用于治疗埃博拉病毒感染者。
吉利德提示,“瑞德西韦是在研药物,这意味着它作为2019-nCoV治疗手段的安全性和有效性尚未被确定。”
目前,瑞德西韦已经在国外通过了Ⅰ期和Ⅱ期临床试验, 目前吉利德正在与国内机构配合,对瑞德西韦用于新型冠状病毒感染进行Ⅲ期临床试验。
成功仿制了一款尚在临床的药物,后续的投放市场依然存在很多不确定性。
首先,瑞德西韦对于新型冠状病毒感染是否有效存在重大不确定性。2月8日吉利德公开表示,瑞德西韦尚未在全球任何国家获得批准,已经与中国卫生部门达成了协议,支持对2019-nCoV感染者开展两项临床试验以确定瑞德西韦(Remdesivir)作为冠状病毒潜在治疗手段的安全性和有效性。
“需要注意的是,瑞德西韦(Remdesivir)是一种试验性药物,迄今为止仅有极少数感染2019-nCoV的患者使用过,因此我们对其疗效尚无足够充分的了解,且目前不足以确保药物能被广泛使用”,吉利德表示。
对此,博瑞医药也在公告中表示,“如果相关临床试验结果不理想,则瑞德西韦的仿制技术就无重大价值可言。”
如果瑞德西韦被证实对新型冠状病毒有效,博瑞医药所生产的仿制药能否投入市场的关键因素,还在于是否得到授权。
博瑞医药表示,公司完成瑞德西韦原料药的仿制和制剂生产后,需经过药物临床试验、药品 审批等多个环节。若瑞德西韦最终**为产品投入市场,需要获得 吉利德公司作为专利权人的授权;这一过程将存在重大不确定性。
值得注意的是,博瑞医药还表示,若该产品能够获批上市,疫情期间主要通过捐赠 等方式供应给相关病人,预计不会对公司 2020 年度经营业绩产生重大影响。
吉利德2016年申请瑞德西韦专利 国内掀起仿制潮?
根据吉利德此前发布的消息,吉利德研发了瑞德西韦,并在美国、中国及世界其他地区拥有专利。2016年,针对瑞德西韦在冠状病毒上的应用,吉利德在中国以及全球申请了更多的专利。在中国,对于冠状病毒应用的专利申请尚待批准。
2月4日,武汉病毒研究所宣布,在1月21日申报了中国发明专利(抗2019新型冠状病毒的用途)后引发热议。2月8日吉利德回应称,“目前,我们关注的重点是尽快确定瑞德西韦(Remdesivir)治疗2019-nCoV感染者的潜在安全性和有效性,并对未来潜在的供应需求加快生产进度。”
一位相关从业者对记者表示,对于瑞德西韦的仿制药能否上市要么只能通过吉利德授权,要么需要通过国家的专利强制许可。
2018年4月,*务*办公厅印发了《关于改*完善仿制药供应保障及使用政策的意见》,其中就提到,要明确药品专利实施强制许可路径,依法分类实施药品专利强制许可,鼓励专利权人自愿许可,必要时国家实施强制许可。
“中国是保护知识产权的,国内到目前为止都没有用过强制许可这个政策,即便是SARS期间都没有用过”,上述从业者表示。
值得注意的是,目前国内或还有其他企业或研究所在研制瑞德西韦的仿制药。
2月10日,瑞德西韦的关键中间体生产商雅本化学在回复投资者问答时表示,“瑞德西韦的两个关键中间体接到多家国内研究所和药厂的询单和订单,朴颐化学有部分库存,也在组织规模生产。”
那么,这些研究所和药厂对瑞德西韦的两个关键中间体下订单所做何用呢?
上述从业者表示,大概率是为了做瑞德西韦仿制药研究。其介绍,吉利德在《Nature》等平台发布了相关的文章,里面就有很多关于瑞德西韦的相关信息,“化合物、分子式都是公布出来的,他要申请专利很多(信息)也是要公布出来的“,”一个化合物你要拿去做研究是干预不了你的,但是他们(吉利德)全球专利都保护好了,研究都可以研究。”
2月11日,有投资者在互动平台向雅本化学了解对瑞德西韦中间体下订单的研究所和厂家名单,公司回应称“客户名称涉及公司商业秘密,不方便公开。公司目前有部分瑞德西韦关键中间体的库存,将立即交付,同时正积极备产以及时向客户供货。 ”
2月12日,新京报记者多次致电雅本化学,电话无人接听。
海南海药完成瑞德西韦制剂靠前批生产 可年产350万支
新京报讯(记者 王卡拉) 2月14日晚间,海南海药发布公告,公司与国内外合作伙伴的紧密合作已完成瑞德西韦原料药及制剂工艺研发,目前已经完成瑞德西韦制剂的靠前批生产, 并已具备年产350万支的规模化生产能力。
瑞德西韦由美国吉利德公司开发,用于防治埃博拉病毒感染,已经在国外通过了Ⅰ期和Ⅱ期临床试验。体外和活体动物试验表明,该药品对多种冠状病毒有效,个别临床病例有效。目前,瑞德西韦正在中国开展用于新型冠状病毒感染的Ⅲ期临床试验,尚未揭盲。因此该药物对于新型冠状病毒感染的治疗是否有效存在重大不确定性。
海南海药称,公司及国内外合作伙伴成功开发了瑞德西韦原料药合成工艺技术和制剂技术,并可量产瑞德西韦原料药,原料药纯度在99%以上。公司已成功完成了瑞德西韦制剂的中试生产,并可批量生产瑞德西韦50mg、100mg两种剂型,已具备瑞德西韦制剂年产350万支的能力。公司可以根据国家安排和社会需要,在符合相关法律法规的前提下随时安排生产,但尚需经过药品审批。
不过海南海药也提醒,公司开发瑞德西韦是为了响应国家号召,尽早获得抗击新冠肺炎疫情的潜在治疗药物。即使瑞德西韦用于新型冠状病毒感染临床试验成功,公司前述研发要最终**为产品投入市场,仍需经过获得专利权人授权、药品审批等多个环节,这一过程将存在重大不确定性。若该产品能够获批上市,预计不会对公司2020年度经营业绩产生重大影响。
还没有批准上市!瑞德西韦临床试验结果4月27日公布
央视网消息: 在昨天(25日)上午举行的*务*联防联控机制新闻发布会上,国家知识产权局副局长何志敏表示,目前,瑞德西韦在任何一个国家都还没有批准上市,现在还处于临床阶段。已在武汉多家医院正式开始的该药物的临床试验,4月27日才能公布临床的试验结果。
国家知识产权局副局长 何志敏 :在媒体上我们也都了解到,瑞德西韦是美国吉利德科学公司正在研发的一款新药,这个药在前期主要用于治疗埃博拉出血热和中东呼吸综合征等疾病,目前这个药在全球的任何一个国家都还没有获批上市,现在还处于临床阶段。我们国家也在武汉的多家医院正式开始了该药物的临床试验,临床试验目前正在进行中,4月27日才能公布临床试验的结果,我们也非常关注这个试验结果。
根据目前公开的情况来看,围绕瑞德西韦,吉利德科学公司的确在中国申请了8件专利,目前已经有3件专利得到授权,还有5件正在审查的过程中。
瑞德西韦加快生产进度 多家上市公司参与合作
证券时报记者 阮润生
针对新型冠状病毒(2019-nCoV)药物研发情况和后续计划,2月7日吉利德科学回复证券时报·e公司记者表示,考虑到当前情况的紧迫性,公司正在采取多种措施加快生产进度,增加供应,另外正与多家机构就未来临床试验的可能性进行讨论。
值得注意的是,日前A股多家医疗上市公司披露与吉利德科学的业务合作情况,部分公司介绍收到吉利德科学有关抗病毒药物中间体的业务询盘以及甚至订单,并提示了风险。
加快生产
据吉利德科学向证券时报·e公司记者回复显示,瑞德西韦作为一种在研的广谱抗病毒药物,尚未在全球任何国家获得批准。针对埃博拉和SARS有限的临床前数据表明,瑞德西韦可能对2019-nCoV具有潜在的活性,并提醒迄今为止仅有极少数感染2019-nCov的患者使用过,因此公司对其疗效尚无足够充分的了解,且目前不足以确保药物能被广泛使用。
目前吉利德科学已与中国卫生部门达成了协议,支持对2019-nCoV感染者开展两项临床试验,以确定瑞德西韦作为冠状病毒潜在治疗手段的安全性和有效性。这两项临床试验由中国研究人员牵头,均在武汉进行。
同时,吉利德科学表示会无偿提供研究所需的药物,并为研究的设计和开展提供支持。
如果初步研究的结果表明瑞德西韦治疗2019-nCoV感染的潜在安全性和有效性,公司会努力制定各种方案,通过适当的渠道将瑞德西韦这种试验性药物向更多患者开放。公司也正与多家机构就未来临床试验的可能性进行讨论。
对于药物库存和生产情况,吉利德科学表示,正在利用库存满足瑞德西韦“同情用药”的需求,以及目前在中国进行的两项临床试验的需求。据介绍,为了应对近年来在西非爆发的埃博拉疫情,吉利德扩大了瑞德西韦的生产,建立了产品库存应对未来的疾病大流行,同时也增加了制造瑞德西韦的原材料库存。
此外,考虑到当前情况的紧迫性,公司正在采取多种措施加快生产进度,增加供应,包括拓展外部制药合作伙伴网络,以加快原材料的采购、原料药和药品的生产;同时,公司开始在内部制造瑞德西韦,以补充外部生产网络产能。
据新华社消息,2月6日晚,抗病毒药物瑞德西韦临床试验已在武汉金银潭医院启动。据瑞德西韦临床试验项目负责人、中日友好医院副院长曹彬教授介绍,总计拟入组761例患者,采用随机、双盲、安慰剂对照方法展开。
另外,瑞德西韦临床试验项目组最新向健康报回应称,临床试验将持续观察随访28天,根据目前进展,顺利的话预计两个月能完成患者入组,整个临床研究结束需要更长时间。
与多家上市公司合作
目前吉利德科学已经上市产品超过25个,覆盖了艾滋病、乙肝、丙肝、心血管疾病、囊性纤维化、呼吸系统疾病和抗真菌等领域,其中在中国市场上市了涵盖丙肝、乙肝以及艾滋病等治疗领域的八款创新药,四款产品已经进入医保。
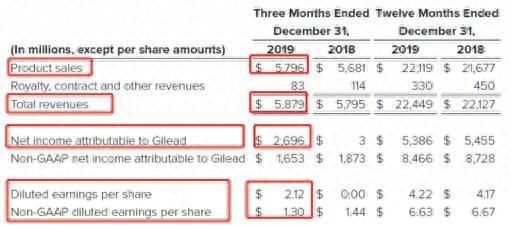
显示,吉利德科学2019年营业收入224亿美元,净利润微降至约54亿美元,研发支出91亿美元,创下公司上市以来*高纪录。
吉利德科学也在加强中国本土合作。吉利德全球CFO Andrew Dickinson曾在进博会上表示,吉利德在中国的策略之一就是与本土的研发创新公司合作。据了解,目前吉利德已经在寻找合作方,期望以后可以通过各种层次的股权合作、股权收购或者是联合研发等进行合作。
日前,已有医药上市公司披露收到了吉利德科学的业务问询函,其中,博腾股份最新披露收到吉利德科学在研抗病毒药物瑞德西韦的中间体订单确认函件。
2月7日晚间公告显示,博腾股份于2月4日已收到核心客户吉利德科学在研抗病毒药物瑞德西韦的中间体订单确认函件;并表示将密切关注瑞德西韦的中国临床试验进程,并积极与吉利德科学团队做好沟通协调,做好全方位的准备。截至目前,该在研药物的相关临床安全性和有效性暂未确认,能否成功治疗新型冠状病毒(2019-nCoV)感染的肺炎存在重大不确定性。
除了博腾股份外,永太科技在2月6日晚公告,公司已收到吉利德关于相关抗病毒药物高级中间体的业务询盘,双方正在洽谈合作事宜,但提示本次是否能达成合作尚存在不确定性,且下游客户在研药物的临床试验和药品获批存在不确定性且需要一定的时间。
另外,也有上市公司澄清与吉利德科学现有业务关系。
九洲药业公告,公司与吉利德于2011年开始合作,公司已为其提供多个品种的医药中间体CDMO服务,近两年,吉利德公司的产品销售收入占公司营业收入不超过2%;同时表示双方尚未未就新型冠状病毒肺炎在研药物瑞德西韦开展实质性合作。
美迪西表示公司与吉利德科学公司2009年开始进行合作,吉利德科学公司是公司的客户之一,但2019年度吉利德科学公司不构成公司的大客户,公司也未直接参与吉利德科学公司的瑞德西韦抗肺炎药物的研发。另外,上海医药表示过与吉利德科学有战略合作关系。
(证券时报记者翁健对本文亦有贡献)
“神药”瑞德西韦背后的传*公司:攻克丙肝 将艾滋治成慢性病

雷达财经出品 文|长帆 编|深海
“前方报道,700多中等和重症患者全部显效!24小时百分之九十六!第二批用药,第三批准备。”2月6日,认证为“长诗‘中国**史诗红旗颂’作者郭某某”的网友微博转发瑞德西韦测试新闻,并配文称,周一之前,三千例第三批全都可用上药。注射针剂,效果就像喷了酒精消毒一样快速彻底。

该微博引发大量网民关注,瑞德西韦真的已经产生效果了吗?2月7日,瑞德西韦临床试验项目组回应,临床试验将持续观察随访28天,顺利的话预计两个月能完成患者入组,整个临床研究结束需要更长时间。
虽然测试结果出炉还需要时间,但瑞德西韦在美国靠前位新型肺炎患者身上疗效明显,该患者已经治愈出院。
瑞德西韦研发公司吉利德堪称传*,攻克丙肝,将艾滋治成慢性病,2019年营收224亿美元。
瑞得西韦治愈美国首例患者
武汉新型肺炎疫情仍未迎来拐点,许多人渴望出现特效药。
1月31日深夜中国科学院辖属的上海药物研究所通过媒体发布:“该所和武汉病毒所联合研究初步发现,中成药双黄连口服液可抑制新型冠状病毒。”
上海药物所对双黄连研究颇深。2003年非典期间,上海药物研究所左建平团队率先证实双黄连口服液具有抗SARS冠状病毒作用。十余年来,左建平团队不间断研究,陆续证实双黄连口服液对流感病毒(H7N9、H1N1、H5N1)、严重急性呼吸综合征冠状病毒(SARS-CoV)、中东呼吸综合征冠状病毒(Middle East Respiratory Syndrome,MERS)具有明显的抗病毒效应。在新型冠状病毒2019-nCoV疫情发生后,上海药物所联合武汉病毒所证实了双黄连口服液对该病毒具有抑制作用。
消息发布后,引发民众对双黄连哄抢,双黄连一度卖断货。
质疑随之而来。2月1日丁香医生发文称,没有足够的公开数据能证明它在人体中“可抑制新型冠状病毒”。人民日报当日早间也发微博提示,“抑制并不等于预防和治疗”。按照世界卫生组织的说法,“到目前为止,还没有用于预防和治疗新型冠状病毒的药物”。
随后,李兰娟院士团队宣布,根据初步测试,在体外细胞实验中显示,阿比朵尔、达芦那韦能有效抑制冠状病毒。但离临床应用,还有相当长的路要走。
在和上海药物所研究所合作的同时,武汉病毒所也在开展其他研究。2月4日,武汉病毒所官网发文称,该所生物安全大科学研究中心与军事科学院军事医学研究院国家应急防控药物工程技术研究中心开展联合研究,在抑制2019新型冠状病毒(2019-nCoV)药物筛选方面取得重要进展。
该研究显示,在Vero E6细胞上,瑞得西韦对2019-nCoV的半数有效浓度EC50=0.77 uM(微摩尔每升),选择指数SI大于129,表明药物在细胞水平上能有效抑制2019-nCoV的感染。
武汉病毒所表示,对在我国尚未上市,且具有知识产权壁垒的药物瑞得西韦,依据国际惯例,从保护国家利益的角度出发,在1月21日申报了中国发明专利(抗2019新型冠状病毒的用途),并将通过PCT(专利合作协定)途径进入全球主要国家。
“如果国外相关企业有意向为我国疫情防控做出贡献,我们双方一致同意在国家需要的情况下,暂不要求实施专利所主张的权利,希望和国外制药公司共同协作为疫情防控尽绵薄之力。”武汉病毒所表示。
2月6日靠前财经记者从吉利德方面*家获悉,吉利德在2016年就已经就该化合物以及针对冠状病毒的用途在全球申请了专利,也包括中国。但是中国的申请还有待批准。
据美国媒体报道,美国首例确诊患者,在接受瑞德西韦治疗后,病情得到有效缓解,《新英格兰医学杂志》发表了该病患详细的确诊过程,该患者在住院后第七天注射瑞德西韦,第二天就不用再吸氧,只有轻微的咳嗽症状,美国专家认为吉利德研制出的这款新药,对冠状病毒具有有效抑制作用。
基于瑞得西韦显现出的疗效。2月5日,中日友好医院王辰、曹彬团队在武汉市金银潭医院宣布启动瑞德西韦治疗新型冠状病毒感染研究。这意味着该抗病毒药物正式进入临床试验。
按照计划,该试验将入组轻、中症患者308例,重症患者453例。曹彬介绍说,这项研究将执行严格的随机双盲试验,以评价瑞德西韦疗效和安全性。
2月6日,微博认证用户郭某某发布微博称瑞德西韦显效,随后获得网友大量转发。2月7日,瑞德西韦临床试验项目组回应,瑞德西韦针对新型冠状病毒感染的III期临床试验由两部分组成,分别评价其在“住院轻-中度肺炎患者”和“住院重症患者”中的疗效与安全性,临床试验将持续观察随访28天。“项目有严格的入排标准,正在争分夺秒推进,根据目前进展,顺利的话预计两个月能完成患者入组,整个临床研究结束需要更长时间”
同济医院呼吸与危重症医学科主任赵建平透露,目前在分组上对重症病人有相应倾斜,“以前分组是1:1,1份治疗用药,1份对照组。这次是2:1,若参加研究有66%的机会用上这个药。”赵建平表示,其他患者不会因为没有用上瑞德西韦延误病情。
丙肝药物疗效太好导致销售下降
公开资料显示,瑞德西韦是一种核苷类似物,具有抗病毒活性,由吉利德公司研发,曾被用于抗埃博拉病毒临床实验。
相比动辄百年历史的欧美医药巨头,吉利德成立时间并不算长。根据公司官网,吉利德科学公司于1987年6月22日注册成立,创始人里奥丹(Michael L Riordan)曾在门罗风险投资公司工作。吉利德是一家以研究为基础,从事药品的开发和销售的生物制药公司。
吉利德成立5年之内,没有收入,8年内没有盈利,外界能看到只是公司一轮又一轮的融资。
当时,奥丹压力非常大,但他依然对旗下的科学家给予全力支持。1992年,吉利德公司的科学家比朔夫贝格尔博士休息时被一张海报所吸引,决心投入到对口服抗流感病毒药物的研究中。为此,比朔夫贝格尔请求吉利德公司成立了以自己为组长的研发小组,小组里包括有机化学家、生物学家、计算机专家等,得到了公司的鼎力支持。
历经三年,比朔夫贝格尔团队才得到初步符合要求的化合物GS4071,小鼠灌胃给药后,发现该药依然存在缺陷,随后继续调整,设计出新的化合物。先在小鼠身上试验,后在大鼠、猴子、雪貂身上进行了实验,药效均非常好。
吉利德和罗氏达成协议,将该药生产和销售权转让给罗氏,该药就是大名鼎鼎的达菲,对流感有奇效,每次流感来临时,都会遭到抢购。

靠着达菲这款“抗流感神药”,吉利德成功翻身。此后,吉利德又推出乙肝、丙肝药物,均非常有效。
Motley Fool网站编辑Keith Speights称,吉利德的丙肝药物疗效如此之高,基本上已经治愈了丙肝。该公司推出推荐丙肝药物Sovaldi时,销售额直线上升。2014年,Sovaldi上市靠前年的全年销售超过了100亿美元。在接下来的3年中,Sovaldi和吉利德开发的后续丙肝药物合计产生了超过430亿美元的销售额。吉利德的丙肝专营权在2015年达到顶峰,但在2017年该公司4款丙肝药物的总销售额已呈断崖式下滑,不足巅峰时期的一半,甚至低于Sovaldi在靠前年上市的销售额。
此外,吉利德推出的艾滋病药物,将艾滋病治成慢性病,最新的药物副作用极低,几乎没耐药。
2019年IDEA Pharma发布全球药企创新指数(Pharmaceutical Innovation Index),吉利德高居榜首。
公司2019年营收224亿美元
根据吉利德中国公司官网,吉利德科学于2007年进入中国,并于2016年建立上海总部。
吉利德在2018年有5个新药在中国获批,是跨国制药企业中获批数量较多的。此外,在2018年CDE公布的《靠前批临床急需境外新药名单》中,吉利德有3款产品入选,是数量第二多的跨国药企。在《第二批临床急需境外新药名单》中,吉利德艾滋病三合一药物比克恩丙诺片同样在列。
2019年,吉利德四个上市一年的新药进入国家医保目录。
截至目前,吉利德已经先后在中国市场上市了涵盖丙肝、乙肝以及艾滋病等治疗领域的八款创新药,而这些新药进入中国市场的时间距FDA批准的美国上市时间,相差最少的不到两年。获批产品数量之多,批准速度之快,在中国医药行业里并不多见。
2019年11月,吉列德公司有4款药物纳入2019年版国家医保目录。根据央视新闻报道,丙肝基因型药品丙通沙(索磷布韦维帕他韦片)首次纳入医保目录后,价格从7万降至1.3万元。
2019《财富》美国500强排名中,吉利德科学公司排在第139位。
2月5日早间,吉利德公布了2019年第四季度和全年财报。公司第四季度营收同比增1.7%,净利润同比暴增近900倍。
以上就是瑞德西韦哪家上市公司生产?海南海药完成瑞德西韦制剂第一批生产的详细内容,希望通过阅读小编的文章之后能够有所收获!更多请关注壹榜财经其它相关文章!
